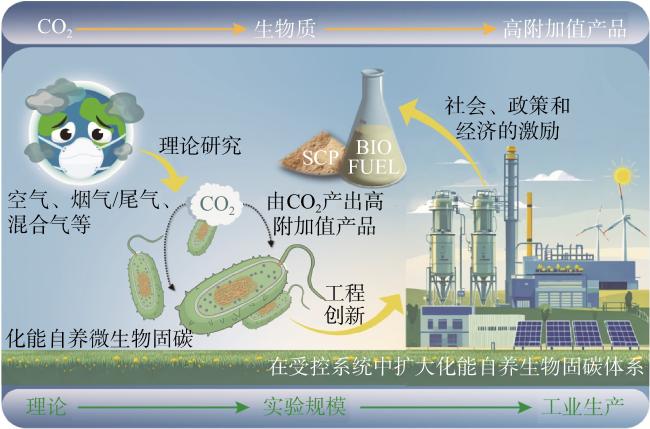
除了生物燃料,单细胞蛋白(single cell protein, SCP)因其高蛋白含量和营养价值越来越受到关注。世界经济论坛第十五届新领军者年会(夏季达沃斯论坛)发布年度《十大新兴技术报告》,其中就包括碳捕获微生物和牲畜饲料蛋白替代技术
[69]。目前,大多数SCP是由异养细菌生产的,这些细菌以碳水化合物、脂类或如CH
4和CH
3OH等底物生长,在此过程中会导致CO
2的产生。相较而言,化能自养细菌的CO
2同化能力使其成为真正可持续SCP生产的最佳候选者,通过化能自养细菌将CO
2转化为SCP可以为农业提供可持续的解决方案。目前,
Clostridium ethanolis生产的微生物蛋白已用于动物饲料,并有望成为新型替代食品蛋白,但需要在生产过程中加入核酸去除步骤
[70]。氢氧化细菌还可以通过在生物反应器中利用水电解产生的H
2作为能源生产单细胞蛋白
[71−72]。然而,这些细菌的生长和培养需要持续的氢气供应,存在风险且生产成本高。何环等
[73]的研究指出,在单质硫中生长的细胞及分离得到的胞外蛋白中富含巯基的蛋白含量明显增加,这表明硫氧化细菌可能是一种潜在的高质量蛋白的生产者。因此,通过化能自养细菌高效转化CO
2为单细胞蛋白是值得关注的一个新的应用方向,进一步研究可从高效菌株的选择、自养微生物蛋白生产的影响因素和机制,以及调控和优化转化过程等关键领域展开。